CRISPR-Cas-Systeme sind die einzigen bekannten adaptiven Immunabwehrsysteme in Bakterien. Sie besitzen die Fähigkeit, genetische Informationen von angreifenden Phagen – Viren, die Bakterien befallen – zu speichern, um zukünftige Infektionen zu bekämpfen. In sogenannten CRISPR-Arrays, also DNA-Sequenzen, wird ein DNA-Schnipsel des Angreifers zwischen zwei festen Sequenzwiederholungen archiviert. Jeder dieser Virus-Schnipsel führt zur Bildung einer CRISPR-Ribonukleinsäure, kurz crRNA (von engl. CRISPR ribonucleic acid), die das System anleitet, denselben Eindringling bei einem erneuten Angriff zu erkennen.
Der zugrunde liegende Mechanismus ist komplex und besteht aus mehreren Komponenten, die gleichzeitig zusammenarbeiten und sich dabei auch gegenseitig beeinflussen können. Ein Beispiel: Damit ein CRISPR-Array gespeichert und korrekt verarbeitet werden kann, muss es mit einer Wiederholungssequenz beginnen und enden. In der Folge entsteht an einem Ende des Strangs eine zusätzliche Wiederholung ohne zugehörigen „Virenschnipsel“. Auch diese wird in eine CRISPR-RNA umgesetzt, allerdings fehlt ihr eine passende Zielsequenz. „Die daraus resultierende CRISPR-RNA, bekannt als ecrRNA (von engl. extraneous CRISPR RNA), ist im besten Fall überflüssig. Schlimmstenfalls lenkt sie die CRISPR-Maschinerien ab und hindert sie daran, nach infizierenden Viren zu suchen“, sagt Chase Beisel, affiliierter Abteilungsleiter am HIRI und Fakultätsmitglied am Botnar Institute of Immune Engineering im schweizerischen Basel. Er hat die Forschungsarbeit, die jüngst in der Fachzeitschrift EMBO Journal erschienen ist, initiiert.
Doch die Natur weiß sich zu helfen: In einer zuvor veröffentlichten Studie in Nature Microbiology aus dem Jahr 2022 hatte ein Team unter Beteiligung von Beisel gezeigt, dass eine Art von CRISPR-Cas-Systemen, die die Nuklease Cas9 zum Schneiden nutzen, durch eine zusätzliche RNA stromaufwärts der problematischen Wiederholung verhindern können, dass sich ecrRNAs bilden. „Die RNA bindet sich an die erste Wiederholung und sorgt dafür, dass diese nicht von der CRISPR-Maschinerie erkannt wird“, erklärt Beisel.
Lange war jedoch unklar, ob auch andere CRISPR-Cas-Systeme von jener Lösung Gebrauch machen. Forschende am Helmholtz-Institut für RNA-basierte Infektionsforschung (HIRI), einem Standort des Braunschweiger Helmholtz-Zentrums für Infektionsforschung (HZI) in Kooperation mit der Julius-Maximilians-Universität Würzburg (JMU), haben gemeinsam mit Wissenschaftler:innen der Universitäten Leipzig, Freiburg und Michigan in den USA untersucht, ob CRISPR-Cas13-Systeme – die wenig Ähnlichkeit mit CRISPR-Cas9-Systemen aufweisen – ecrRNAs produzieren und, falls ja, wie sie diesen entgegenwirken.
Eine systemübergreifende Lösung
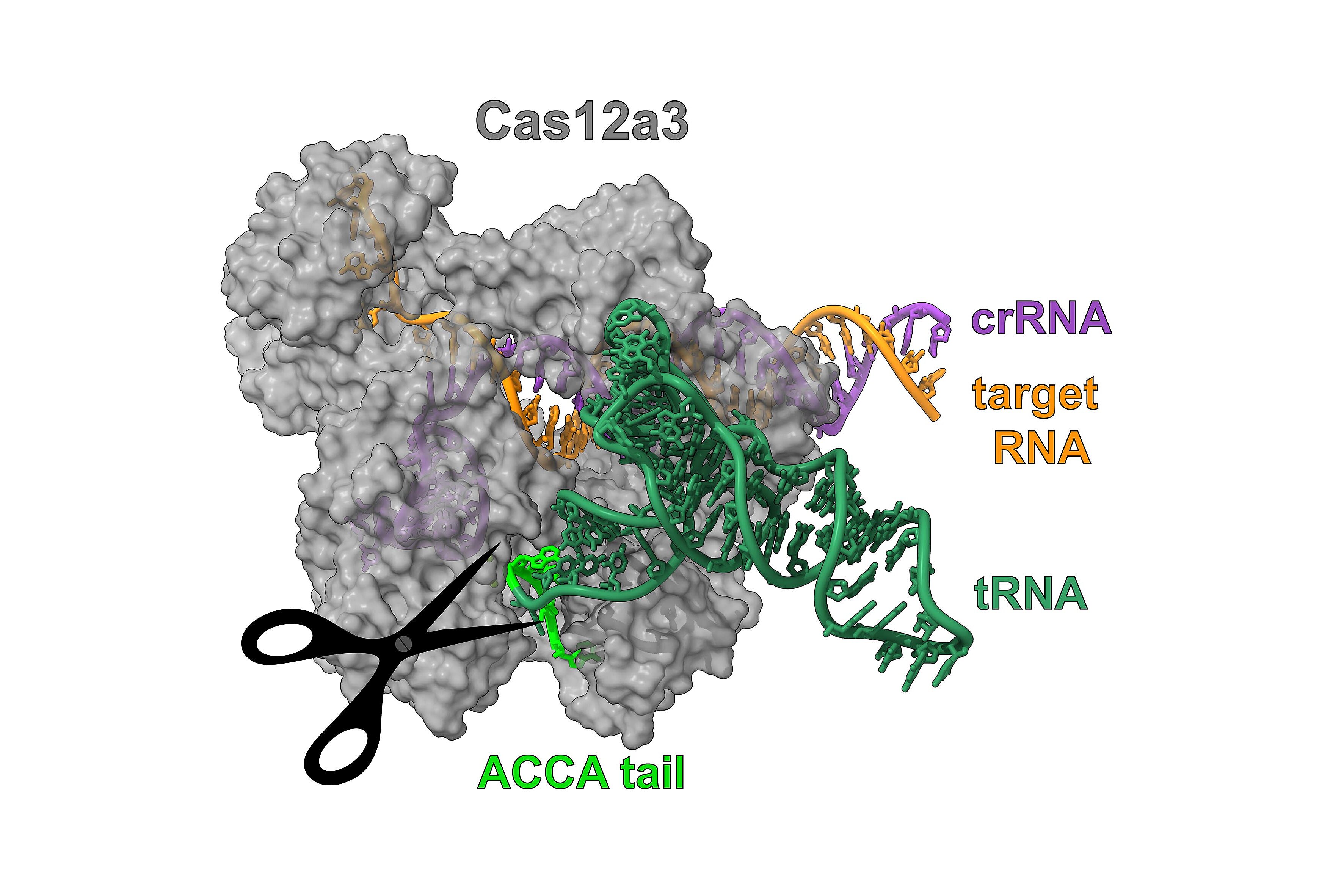
„Wir konnten herausfinden, dass viele CRISPR-Cas13-Systeme ebenfalls über RNA verhindern, dass sich ecrRNAs bilden“, sagt Angela Migur, ehemalige Postdoktorandin im Labor von Chase Beisel. Die schützende RNA formt in der ersten Wiederholung eine stabile Struktur, die einer Haarnadelstruktur ähnelt. Diese verhindert, dass sich die Cas13-Nuklease an die Wiederholung binden, sie verarbeiten und so eine ecrRNA herstellen kann. „Das Auftreten der ‚Haarnadel‘ war unerwartet, da sich CRISPR-Cas9- und CRISPR-Cas13-Systeme unabhängig voneinander entwickelt haben und sehr unterschiedlich funktionieren“, fügt Migur hinzu. „Überraschenderweise waren die Mechanismen, die die ecrRNA-Bildung verhinderten, allerdings sehr ähnlich.“
Diese Beobachtungen deuten auf einen bemerkenswerten Fall konvergenter Evolution hin: Verschiedene CRISPR-Cas-Systeme haben unabhängig voneinander Mechanismen entwickelt, um gemeinsame Hürden in der Immunabwehr zu überwinden.
Das Team konnte außerdem feststellen, dass nicht alle CRISPR-Cas-Systeme auf eine solche schützende RNA zurückgreifen. Ausschlaggebend war dabei, ob die zusätzliche Wiederholung am Anfang oder am Ende des CRISPR-Arrays auftrat. Diese Beobachtung deutet darauf hin, dass es noch weitere unterschiedliche Strategien zu entdecken gibt, welche die Wirkweise von CRISPR-Cas-Systemen verbessern.
Neue Forschungsperspektiven
Cas13-Nukleasen werden heute häufig als Forschungswerkzeuge sowie als nicht permanente Methode zur Geneditierung auf RNA-Ebene eingesetzt. Die neue Entdeckung des Forschungsteams könnte dazu beitragen, diese Systeme besser nutzbar zu machen, indem sichergestellt wird, dass ausschließlich die beabsichtigten CRISPR-RNAs gebildet werden. Darüber hinaus besteht die Möglichkeit, die virale Abwehr durch das CRISPR-Cas-System mithilfe von ecrRNAs zu hemmen, wodurch sich das genetische Werkzeug leichter kontrollieren lässt.
Die Forschung hat zwar bereits enorme Anstrengungen unternommen, um neue CRISPR-Cas-Systeme zu charakterisieren. Dabei konzentrierte man sich allerdings vor allem auf die grundlegenden Mechanismen der adaptiven Immunität, insbesondere auf die Eigenschaften der jeweiligen Nukleasen. Jedoch ist bislang kaum untersucht, wie die einzelnen Komponenten dieser Systeme optimal aufeinander abgestimmt sind, um ihr Zusammenspiel möglichst effizient zu gestalten. In dieser Arbeit wurde ein Schwachpunkt des Prinzips der CRISPR-Arrays aufgedeckt, der sich aber leicht durch eine einfache Haarnadel-RNA beheben lässt. „Wir hoffen, dass unsere Arbeit die Forschungsgemeinschaft dazu anregt, die Einschränkungen von CRISPR-Cas-Systemen und anderen bakteriellen Abwehrmechanismen intensiver zu untersuchen. Zugleich gilt es zu klären, welche Strategien diese Systeme entwickelt haben, um solche Hürden möglichst effektiv zu überwinden“, so Beisel.