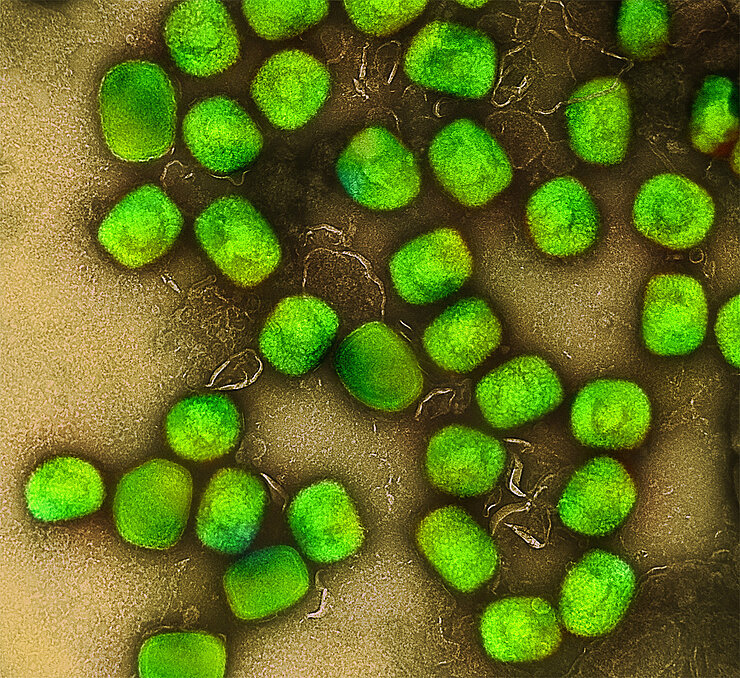
Mpox
Ein globaler Ausbruch hat Mpox im Jahr 2022 weltweit auf den Radar gebracht. Die Viruserkrankung, die vom Monkeypox-Virus (MPXV) ausgelöst wird, kann sowohl zoonotisch von Tieren auf Menschen übertragen werden als auch zwischen Menschen. Das Virus ist in West- und Zentralafrika endemisch, durch verschiedene Ausbrüche mittlerweile aber global verbreitet. Die Infektion verläuft meistens mild. Sie kann für Kinder, Schwangere und Menschen mit Vorerkrankungen aber auch schwer bzw. tödlich verlaufen. Neben allgemeinen Krankheitssymptomen wie Fieber, Abgeschlagenheit und Muskelschmerzen verursacht das MPXV schmerzhafte Hautläsionen.
MPXV zirkuliert in zwei Hauptkladen, Kladen I und II – jeweils mit den Subkladen a und b –, die sich hinsichtlich Virulenz, genetischer Merkmale und Epidemiologie deutlich voneinander unterscheiden. Die Klade I wurde in der Vergangenheit mit schwereren Krankheitsverläufen und einer höheren Sterblichkeitsrate in Verbindung gebracht, während die Klade II im Durchschnitt mildere Krankheitsverläufe verursacht. Der weltweite Ausbruch im Jahr 2022 wurde durch die Klade IIb ausgelöst, die bei immunkompetenten Personen durch weniger systemische Symptome gekennzeichnet ist. Dies könnte eine verstärkte Übertragung von Mensch zu Mensch begünstigt haben, doch werden auch eine virale Anpassung und eine Veränderung der Expositionswege diskutiert. Die Klade Ib, die zuletzt aufgetretene MPXV-Subklade, zeigt ebenfalls Anzeichen einer anhaltenden Übertragung von Mensch zu Mensch. Der Übergang von einer historisch zoonotischen, lokal begrenzten Übertragung zu einer anhaltenden Mensch-zu-Mensch-Verbreitung, vor allem auch über sexuellen Kontakt, markiert eine bedeutende Veränderung in der MPXV-Epidemiologie.
Mpox kann über Haut- und Schleimhautkontakt sowie über Gegenstände oder Oberflächen übertragen werden. Ob auch eine Tröpfchenübertragung möglich ist und ob sich die Anfälligkeit für eine Infektion je nach Übertragungsweg ändert, ist noch nicht wissenschaftlich geklärt. Um diese und weitere Forschungsfragen zur MPXV-Übertragung zu klären, entwickelt Dr. Julia Port mit ihrer Forschungsgruppe „Transmissionsimmunologie“ am Helmholtz-Zentrum für Infektionsforschung (HZI) Labor- und Tiermodelle für Mpox. Sie hat die Vielzitzenmaus (Mastomys natalensis), ein kleines Nagetier, das in weiten Teilen Afrikas verbreitet ist, als Mpox-Tiermodell etabliert und konnte zeigen, dass der Übertragungsweg entscheidend dafür ist, welches Krankheitsbild sich ausbildet. Beispielsweise verursacht MPXV Klade IIb im Tiermodell nur milde Symptome, wenn es in die Bauchhöhle verabreicht wird. Bei mukosaler (rektaler oder vaginaler) Exposition ist das Krankheitsbild ausgeprägter und kommt der Mpox-Erkrankung beim Menschen näher. Zudem scheiden die infizierten Tiere mehr Virus aus. „Wir brauchen ausgefeiltere Modelle, die die Übertragungs- und immunpathologischen Prozesse nachbilden, die wir untersuchen wollen. Das mag banal klingen, ist aber eine wichtige Voraussetzung, damit wir Rückschlüsse auf den Menschen ziehen können“, sagt Port. Mithilfe von Haut- und Lungenorganoiden untersuchen Forscher:innen des HZI zudem die Mechanismen, wie MPXV vom Immunsystem erkannt wird und wie das Virus den Immunzellen entgeht. Organoide sind aus Stammzellen erzeugte Miniaturmodelle von Organen, die räumlich und strukturell den tatsächlichen Organen ähneln.
Impfschutz gegen Mpox
In der EU ist ein modifizierter Pockenimpfstoff zur Mpox-Prävention zugelassen. Dieser kann innerhalb der ersten Tage nach dem Kontakt mit Erkrankten auch als Postexpositionsprophylaxe (PEP) eingesetzt werden. MPXV ist mit dem mittlerweile ausgerotteten Variola-Virus, dem Erreger der Pocken, verwandt. Durch Kreuzimmunität schützt eine Pockenimpfung daher teilweise auch gegen Mpox. Nach der Ausrottung des Pockenvirus wurde die Pockenimpfpflicht 1976 in der BRD und 1982 in der damaligen DDR aufgehoben. Daher haben große Bevölkerungsgruppen keine Pockenimmunität mehr. Das Windpockenvirus gehört trotz des Namens nicht zur Familie der Pockenviren, sondern zu den Herpesviren. Eine Windpockeninfektion oder –impfung bietet daher auch keinen Schutz vor Mpox.
Feuerfußhörnchen als Mpox-Reservoir
Mitglieder der Gattung der Pockenviren treten in vielen verschiedenen Säugetierspezies auf. Die einzelnen Pockenvirus-Arten haben jedoch in der Regel ein enges Wirtsspektrum. Während sich das Variola-Virus evolutionär an den Menschen angepasst hat, ist MPXV ursprünglich ein Tiervirus. Gezielte Präventionsmaßnahmen werden aber dadurch erschwert, dass nur wenig darüber bekannt ist, in welchen Tieren das Virus zirkuliert. Ein Durchbruch gelang Forscher:innen des Helmholtz-Instituts für One Health (HIOH), als sie ein Tierreservoir des Virus identifizieren konnten. Dafür untersuchten sie einen Mpox-Ausbruch unter wildlebenden Rußmangaben im Taï-Nationalpark in Côte d’Ivoire. Gemeinsam mit dem Taï Chimpanzee Project und weiteren Partnern kombinierten sie ökologische, verhaltensbezogene und molekulare Daten und konnten zeigen, dass das Virus durch den Verzehr von infizierten Feuerfußhörnchen auf die Primaten übertragen wurde. „Wenn wir tierische Virusquellen und Wege, die zur Übertragung zwischen Arten führen, kennen, können wir Spillover-Mechanismen besser verstehen. So können wir wirksame Präventionsmaßnahmen entwickeln, die das Risiko einer Übertragung auf den Menschen verringern“, sagt Prof. Fabian Leendertz, Gründungsdirektor des HIOH, der seit vielen Jahren Mpox in verschiedenen Säugetierspezies untersucht.
Forscher:innen des HIOH betreiben gemeinsam mit lokalen Partnern in der Zentralafrikanischen Republik und in Côte d’Ivoire Aufklärung in der Bevölkerung. Sie informieren etwa über die Infektionsrisiken, die vom Kontakt mit bestimmten Tierarten wie Feuerfußhörnchen ausgehen. Zudem unterstützen sie beim Aufbau der Diagnostik für Mpox und andere Infektionskrankheiten, um Ausbrüche schneller kontrollieren zu können. Ebenfalls zur Kontrolle von Ausbrüchen trägt das am HZI entwickelte digitale Tool SORMAS (Surveillance, Outbreak Response Management and Analysis System) bei. Es enthält ein Mpox-Modul und hilft bei der Erfassung von Daten zu Übertragungswegen sowie der geographischen Verteilung von Infektionsfällen.
Die Mpox-Forschung am HZI ist nicht nur wissenschaftlich bedeutend, sondern auch unmittelbar praxisrelevant. Durch die Entwicklung präziser Tiermodelle, die Identifikation von Tierreservoirs und die Unterstützung von Diagnostik- und Präventionsmaßnahmen trägt das HZI entscheidend dazu bei, Spillover-Ereignisse zu verstehen und zukünftige Ausbrüche zu verhindern oder frühzeitig zu erkennen. So lassen die Forscher:innen des HZI wissenschaftliche Erkenntnisse direkt in wirksame Maßnahmen münden.
Stand: März 2026
(cwe)
Weitere Informationen
- Mpox-Informationsseite des Bundesinstituts für Öffentliche Gesundheit;
- HZI-Podcast InFact mit Julia Port: Wie sich Viren verbreiten – Mpox, Transmissionsimmunologie und globale Gesundheit
Beteiligte Forschungsgruppen
-
Evolution von Krankheitserregern
 Prof. Dr. Sébastien Calvignac-Spencer
Prof. Dr. Sébastien Calvignac-Spencer -
Ökologie und Entstehung von Zoonosen
 Prof. Dr. Fabian Leendertz
Prof. Dr. Fabian Leendertz -
Transmissionsimmunologie
 Dr. Julia Port
Dr. Julia Port