Wissenschaftler*innen des Deutschen Primatenzentrums – Leibniz-Institut für Primatenforschung (DPZ, Göttingen) haben zusammen mit Partnern an der Charité (Berlin), der Medizinischen Hochschule Hannover, des Helmholtz-Zentrums für Infektionsforschung (Braunschweig) und der Friedrich-Alexander-Universität Erlangen-Nürnberg die biologischen Eigenschaften der Pirola-Variante untersucht. Die Forschenden haben herausgefunden, dass die Pirola-Variante im Gegensatz zu den vorher zirkulierenden Omikron-Varianten mit hoher Effizienz in Lungenzellen eindringt und dafür das zelluläre Enzym TMPRSS2 verwendet. Damit weist die Pirola-Variante überraschende Parallelen zu den in den ersten Jahren der Pandemie zirkulierenden Varianten Alpha, Beta, Gamma und Delta auf. Das verbesserte Eindringen in Lungenzellen könnte auf ein aggressiveres Virus hindeuten, allerdings war die Bildung neuer, infektiöser Viren durch infizierte Zellen reduziert, was Ausbreitung und pathogenes Potenzial vermindern könnte. Schließlich berichten die Forschenden, dass die Pirola-Variante gegen alle verfügbaren therapeutischen Antikörper resistent ist und auch Antikörpern in geimpften Personen mit und ohne Durchbruchinfektion effizient ausweicht. Allerdings wird das Virus gut durch Antikörper gehemmt, die durch den neuen, XBB.1.5-angepassten mRNA-Impfstoff hervorgerufen werden. Zusammenfassend zeigen die Ergebnisse, dass sich auch vier Jahre nach Beginn der Pandemie das Virus massiv verändern und dabei Eigenschaften wiedergewinnen kann, die die Entstehung einer schweren Erkrankung fördern können.
Die Ausbreitung von SARS-CoV-2 ist mit der ständigen Entstehung neuer Virus-Varianten verbunden. Diese Varianten haben Mutationen im Spike Protein erworben, die es ihnen ermöglichen, neutralisierenden Antikörpern in Geimpften und Genesenen auszuweichen. Die Entwicklung von Virus-Varianten begann mit der Alpha-Variante, gefolgt von der Beta-, Gamma- und Delta-Variante. Ende 2021 wurde die Omikron-Variante weltweit dominant, die sich genetisch stark von den vorher zirkulierenden Varianten unterschied. Für diese starke Veränderung musste das Virus jedoch einen Preis bezahlen. Die Omikron-Variante kann sich neutralisierenden Antikörpern hochwirksam entziehen und wird sehr effizient übertragen, aber sie hat die Fähigkeit verloren, ein Schlüsselenzym der Wirtszelle, die Protease TMPRSS2, für den Eintritt in Lungenzellen effizient zu nutzen. Daher löst die Omikron-Variante weniger häufig eine Lungenentzündung aus.
Pirola: Quantensprung in der SARS-CoV-2 Evolution
Abkömmlinge der Omikron-Variante waren bis Ende 2023 global dominant. Neue Varianten unterschieden sich häufig nur durch wenige Mutationen von ihren Vorgängern und es gab Hinweise darauf, dass die im Jahr 2023 zirkulierenden Viren nur noch begrenzte Möglichkeiten hatten, sich dem Antikörperdruck in der Bevölkerung zu entziehen. Die Entdeckung einer neue SARS-CoV-2 Omikron-Untervariante, Pirola (BA.2.86), die sich genetisch sehr stark von anderen zirkulierenden Viren unterscheidet, hat daher große Aufmerksamkeit erregt. Die Pirola-Variante ist vermutlich, analog zur Omikron-Variante, in immungeschwächten Patienten entstanden und stellt einen Quantensprung in der SARS-CoV-2 Evolution dar. Das Spike-Protein der Pirola-Variante trägt mehr als 30 Mutationen im Vergleich zur Vorgänger-Variante, BA.2, und es ist unklar, wie diese Mutationen die biologischen Eigenschaften des Virus beeinflussen. Ein Forscherteam des Deutschen Primatenzentrums (DPZ) um Markus Hoffmann und Stefan Pöhlmann hat diese Frage zusammen mit den Arbeitsgruppen von Christan Drosten (Charité, Berlin), Georg Behrens (Medizinische Hochschule Hannover), Luka Cicin-Sain (Helmholtz-Zentrum für Infektionsforschung, Braunschweig) und Hans-Martin Jäck (Friedrich-Alexander-Universität, Erlangen) untersucht.
Pirola kann Lungenzellen effizienter infizieren…
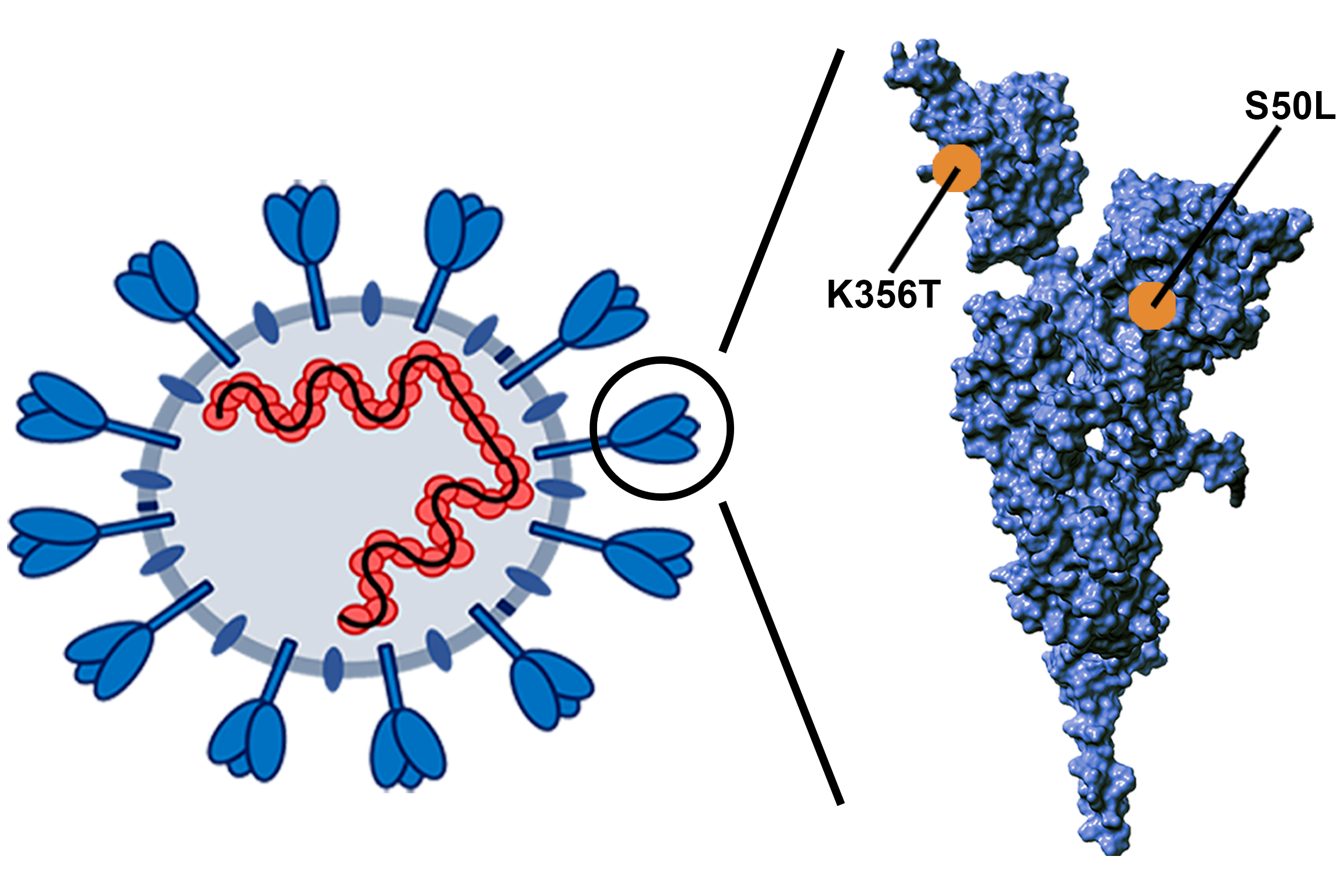
Die Forschenden fanden heraus, dass die Pirola-Variante im Gegensatz zu allen vorher zirkulierenden Omikron-Untervarianten hocheffizient in Lungenzellen eindringen kann und dafür TMPRSS2 verwendet. Außerdem konnten sie zeigen, dass die Mutationen S50L und K356T im Spike-Protein der Pirola-Variante für den hocheffizienten Eintritt in Lungenzellen wichtig sind. „Es ist bemerkenswert, dass sich zwei Jahre nach globaler Dominanz der Omikron-Variante, die nicht effizient in Lungenzellen eindringt, nun ein stark verändertes Virus ausbreitet, das wieder effizient in Lungenzellen eindringen kann. Ob der verstärkte Lungenzelleintritt mit stärkerer Krankheit nach Infektion mit der Pirola-Variante verbunden ist, müssen Studien in Tierversuchen zeigen“, sagt Stefan Pöhlmann, Leiter der Abteilung Infektionsbiologie am Deutschen Primatenzentrum.
… sich aber weniger gut vermehren, als ihre Vorgänger
SARS-CoV-2-infizierte Zellen bilden neue Virus-Partikel, von denen viele, aber nicht alle, neue Zellen infizieren können. Die Forschenden fanden Hinweise darauf, dass Zellen, die mit der Pirola-Variante infiziert wurden, weniger effizient neue, intakte Virus-Partikel bilden als Zellen, die mit zuvor zirkulierenden Varianten infiziert wurden. „Die relativ ineffiziente Bildung von infektiösen Virus-Partikeln durch Zellen, die mit der Pirola-Variante infiziert wurden, war überraschend“, sagt Markus Hoffmann, der Ansprechpartner für diese Studie. „Es wird interessant sein zu erforschen, welcher Mechanismus dafür verantwortlich ist. Möglicherweise handelt es sich um die Bildung von defekten interferierenden Partikeln, die die Ausbreitung der Pirola-Variante regulieren und zur Antikörperflucht beitragen.“
Therapeutische Antikörper unwirksam gegen Pirola-Variante
Für die COVID-19 Prophylaxe und Therapie werden im Labor hergestellte, neutralisierende Antikörper eingesetzt. Da die Viren an den Antikörperbindestellen mutieren, sind jedoch die meisten dieser Antikörper gegen aktuell zirkulierende Varianten nicht wirksam. Die aktuelle Studie zeigt, dass die Pirola-Variante keine Ausnahme darstellt – keiner der getesteten Antikörper konnte das Virus hemmen. „Diese Ergebnisse zeigen, dass die Entwicklung von neuen Antikörpern mit sehr breiten Wirkspektrum wichtig ist“, sagt Markus Hoffmann.
Neuer, angepasster Impfstoff schützt vor Pirola
Die Pirola-Variante konnte auch Antikörpern ausweichen, die nach Impfung oder Infektion gebildet wurden, allerdings weniger effizient als die parallel zirkulierende Eris-Variante (EG.5.1). Antikörper, die nach Impfung mit dem neuen XBB.1.5-adaptieren Impfstoff generiert wurden, konnten dagegen sowohl die Pirola- als auch die Eris-Variante gut hemmen. „Diese Ergebnisse zeigen, dass der XBB.1.5-adaptierte Impfstoff einen robusten, wenn auch wahrscheinlich nur temporären Schutz gegen die Infektion mit der Pirola-Variante aufbauen könnte“, sagt Markus Hoffmann. „Dabei ist es interessant, dass eine Untervariante von Pirola gegenwärtig global auf dem Vormarsch ist, die eine weitere Mutation im Spike-Protein trägt, die die Antikörperflucht verstärken könnte. Das Virus ist also dabei, sich zu optimieren und die Folgen dieser Optimierung sollten untersucht werden“, ergänzt Lu Zhang, Erstautorin der Studie.